Wszyscy wiemy, że woda jest świetnym rozpuszczalnikiem przeróżnych substancji, może rozpuszczać także gazy a wśród nich i tlen. Ale co zrobić jeśli chcemy się dowiedzieć ile tlenu rozpuściło się w wodzie? np. w stawie rybnym by sprawdzić czy ryby nie zaczną pływać do góry brzuszkami? - odpowiedź jest prosta - należy przeprowadzić analizę ilościową.
Jest wiele metod oznaczania rozpuszczonego w wodzie tlenu. Ja przedstawię metodę, którą poznałem bardzo dokłądnie w szkole średniej. Jest to tzw. metoda Winklera.
Pierwszą czynnością badania jest pobranie próbki wody. W tym celu potrzebna będzie szklana butelka o poj. ok. 250 cm3. Gdy pobierzemy już wodę wprowadzamy do niej mangan jako roztwór MnSO4, a następnie zasadowy roztwór jodku potasu. Po tej czynności mangan wytrąca się w postaci kłaczkowatego, biełego osadu Mn(OH)2 zgodnie z równaniem:
Mn2+ + 2 OH- = Mn(OH)2 - biały osad
Zawarty w badanej próbce rozpuszczony tlen utlenia jony Mn(II) do Mn(IV) zgodnie z równaniem:
2 Mn(OH)2 +O2 = 2 MnO(OH)2 - jasnobrązowy osad
W środowisku kwaśnym pod wpływem Mn(IV) wydziela się z wcześniej dodanego jodku potasu wolny jod w ilości równoważnej do zawartości tlenu w badanej próbce zgodnie z równaniami:
MnO(OH)2 + 4 H+ = Mn4+ + 3 H2O
Mn4+ + 2 I- = Mn2+ + I2
Wydzielony wolny jod oznacza się metodą miareczkowania za pomocą tiosiarczanu(VI) sodu wobec skrobi jako wskaźnika. Ilość wydzielonego jodu jest wprost proporcjonalna do rozpuszczonego w badanej próbce tlenu.
I2 + 2 S2O32- = 2 I- + S4O62-
Z ilości zużytego mianowanego roztworu tiosiarczanu sodu oblicza się zawartość tlenu rozpuszczonego w wodzie.
Potrzebne odczynniki:
 1. Zasadowy roztwór jodku potasu (zdjęcie po lewej przedstawia potrzebne do przygotowania tego odczynnika chemikalia i szkło)- W kolbie miarowej o poj. 100 cm3 rozpuszczamy w jak najmniejszej ilości wody 15 g jodku.
1. Zasadowy roztwór jodku potasu (zdjęcie po lewej przedstawia potrzebne do przygotowania tego odczynnika chemikalia i szkło)- W kolbie miarowej o poj. 100 cm3 rozpuszczamy w jak najmniejszej ilości wody 15 g jodku.
 Przygotowujemy naważkę a następnie przy pomocy małego lejka i tryskawki przenosimy ją ilościowo do kolbki miarowej.
Przygotowujemy naważkę a następnie przy pomocy małego lejka i tryskawki przenosimy ją ilościowo do kolbki miarowej.
 (obraz po lewej przedstawia jak powinno się przenosić naważkę do kolby miarowej.)
(obraz po lewej przedstawia jak powinno się przenosić naważkę do kolby miarowej.)
 Teraz w oddzielnym naczyniu rozpuszczamy 70 g wodorotlenku potasu. Przy tej czynności musimy zachować szczególną ostrożność. Wodorotlenek potasu jest silnie żrący a podczas rozpuszczania go w wodzie roztwór bardzo silnie się rozgrzewa. Nie ma nic gorszego niż gorący, silnie żrący roztwór !!!.
Teraz w oddzielnym naczyniu rozpuszczamy 70 g wodorotlenku potasu. Przy tej czynności musimy zachować szczególną ostrożność. Wodorotlenek potasu jest silnie żrący a podczas rozpuszczania go w wodzie roztwór bardzo silnie się rozgrzewa. Nie ma nic gorszego niż gorący, silnie żrący roztwór !!!.
 Po rozpuszczeniu wodorotlenku potasu, rozrwór musimy koniecznie wystudzić do temperatury pokojowej a następnie przelać do wcześniej sporządzonego roztworu jodku potasu w kolbie miarowej. Roztwory mieszamy ze sobą i dopełniamy wodą destylowaną do kreski. Mamy już gotowy pierwszy potrzebny nam do oznaczenia odczynnik - zasadowy roztwór jodku potasu.
Po rozpuszczeniu wodorotlenku potasu, rozrwór musimy koniecznie wystudzić do temperatury pokojowej a następnie przelać do wcześniej sporządzonego roztworu jodku potasu w kolbie miarowej. Roztwory mieszamy ze sobą i dopełniamy wodą destylowaną do kreski. Mamy już gotowy pierwszy potrzebny nam do oznaczenia odczynnik - zasadowy roztwór jodku potasu.
 Przygotowany odczynnik jest wrażliwy na światło, które powoduje jego rozkład z wydzieleniem wolnego jodu. Odczynnik należy przelać do butli z ciemnego szkła.
Przygotowany odczynnik jest wrażliwy na światło, które powoduje jego rozkład z wydzieleniem wolnego jodu. Odczynnik należy przelać do butli z ciemnego szkła.
Kolejne, potrzebne do oznaczenia odczynniki.
Następnym potrzebnym do oznaczenia odczynnikiem będzie stężony roztwór siarczanu manganu MnSO4 x 5H2O.

Rys: Odważona ilość pięciowodnego siarczanu manganu.
W celu przygotowania potrzebnego do oznaczenia odczynnika odważamy 52g pięciowodnego siarczanu manganu MnSO4 x 5H2O i rozpuszczamy w kolbie miarowej w 100 ml wody destylowanej.

Rys: Odważka przeniesiona do kolby miarowej.
Po przeniesieniu substancji do kolby miarowej i jej rozpuszczeniu, roztwór należy jeszcze przesączyć i umieścić w butli ze szlifowanym korkiem.
I kolejny odczynnik - stężony kwas siarkowy H2SO4. Specjalnie nie trzeba go przygotowywać, jednak jeśli posiadamy go większą ilość, dobrze jest przelać ok 100 ml do innej szklanej butli. Zapobiegnie to ewentualnemu zanieczyszczeniu całej posiadanej objętości i w razie wypadku straty będą mniejsze.

Rys: Stężony kwas siarkowy.
Potrzebny będzie jeszcze roztwór skrobi. w tym celu niewielką ilość skrobi zalewamy wrzącą wodą w zlewce i jeszcze przez chwilkę gotujemy. Roztwór studzimy i przelewamy do pojemnika, w którym będzie przechowywany. Dla zabezpieczenia przed ewentualnym rozwojem w nim drobnoustrojów dolewamy 1 ml alkoholu.
Wszystkie przedstawione powyżej roztwory mogły być przygotowywane nieco mniej starannie bo stężenie ich nie musi być dokładnie znane. W oznaczeniu biorą udział w nadmiarze. Natomiast odczynnik, który teraz przygotujemy musi mieć dokładnie określone miano tzn. jego stężenie musi być bardzo dokładnie znane. Im mniej dokładnie przygotujemy ten roztwór tym mniej dokładnie oznaczymy rozpuszczony w wodzie tlen. Ale o tym na następnej stronie.
Odczynnikiem, który musimy przygotować starannie jest mianowany roztwór tiosiarczanu sodu o stężeniu 0,1 mol x dm-3. Mianowane roztwory o dokładnie znanym stężeniu przygotowuje się odważając na wadze analitycznej z bardzo dużą dokładnością (często z dokładnością nawet do 4 miejsca po przecinku) potrzebną ilość substancji dla otrzymania konkretnego stężenia i rozpuszcza w dokładnie znanej ilości wody.
Pięciowodny tiosiarczan sodu jest jednak bardzo niewdzięczną substancją, która potrafi szybko zmieniać swoją masę - traci lub pozyskuje część swojej wody hydratacyjnej. Jego roztwór przygotowuje się poprzez odważenie ilości substancji z mniejszą dokładnością a miano roztworu ustala się poprzez przeprowadzenie innej analizy.
Ja z natury jestem raczej leniwy więc do przygotowania roztworu wykorzystam inny sposób. Firmy produkujące odczynniki sprzedają je także w tzw. fiksanalach . Są to zatopione rurki szklane z bardzo dokładnie odważoną ilością substancji.

Rys: Fiksanal zawierający 24, 820 g pięciowodnego tiosiarczanu sodu.
Fiksanal, który zakupiłem zawiera dokładnie 0,1 mola tiosiarczanu sodu czyli 24, 820 g czystej substancji. Świetna sprawa bo teraz wystarczy przenieść tę substancję ilościowo do kolby miarowej o poj. 1 dm3 i dopełnić wodą destylowaną do kreski. Otrzymamy mianowany roztwór tiosiarczanu sodu o stężeniu 0,1 mol x dm-3
Poniżej przedstawiam wszystkie przygotowane wcześniej odczynniki, dzięki którym oznaczymy w badanej wodzie tlen rozpuszczony.

Rys: Wszystkie przygotowane odczynniki.
Pierwszą czynnością jaką wykonamy będzie rozcieńczenie 0,1 molowego r-r tiosiarczanu sodu. Stężenie 0,1 mol x dm3 jest trochę za duże i mogło by sprawiać kłopoty przy miareczkowaniu - zbyt mała ilość roztworu spowodowała by odbarwienie i tym samym dokładność by się zmniejszyła. Do oznaczenia potrzebować będziemy roztworu o stężeniu 0,025 mol x dm3 czyli musimy zastosować rozcieńczenie 1+3.
Rozcieńczenie to będzie bardzo proste gdy mamy do dyspozycji kolbę miarową o poj. 100 cm3 i jednomiarową pipetę o poj 25 cm3. Kolba miarowa musi być sucha, ja świeżo ją umyłem więc muszę wysuszyć np. opalarką elektryczna lub suszarką. Musimy pamiętać by ogrzewać kolbę i wszystkie inne szkła miarowe bardzo delikatnie !.

Rys: Suszenie kolby miarowej.
Wreszcie zaczynamy badać zawarty w wodzie tlen.
Teraz pipeta jednomiarowa. Jest to szklana rurka z wygrawerowaną kreską znaczącą objętość 25 cm3

Rys. Pipeta jednomiarowa o poj. 25 cm3
Za pomocą pipety jednomiarowej zaciągamy 25 cm3 wcześniej przygotowanego 0,1 molowego roztworu tiosiarczanu i przenosimy do wysuszonej wcześniej kolby miarowej.

Rys. Przenoszenie 25 cm3 0,1 molowego r-r tiosiarczanu sodu.
Kolbę dopełniamy wodą destylowaną do kreski i mamy 100 cm3 r-r o stężeniu 0,025 mol x dm-3, który zastosujemy do miareczkowania wydzielonego jodu w badanej próbce.
Wreszcie po wielu czynnościach przygotowawczych możemy przystąpić do właściwego badania. Na początek potrzebna nam będzie mała kolbka z doszlifowanym korkiem.

Rys. Kolbka z doszlifowanym korkiem, w której przeprowadzimy reakcje.
Wodę do badania np. z rzeki pobieramy w ten sposób by nie dopuścić do rozpuszczenia kolejnej porcji tlenu podczas naszych czynności. Otwartą kolbkę zanurzamy całkowicie w wodzie, czekamy aż się wypełni i zamykamy ją korkiem pod wodą.
Teraz do tak pobranej wody dodajemy najpierw 1 cm3 roztworu siarczanu manganu.

Rys. Do badanej próbki dodajemy r-r siarczanu manganu.
Teraz do próbki dodajemy roztwór jodku potasu w ilości 2 cm3 i wreszcie zaczyna się coś dziać.

Rys: Dodanie r-r jodku potasu w środowisku zasadowym powoduje wytrącenie kłaczkowatego osadu zgodnie z przedstawionym wcześniej równaniem.
Biały osad wytrąca się i od razu utlenia się rozpuszczonym tlenem, co powoduje zabarwienie jasnobrązowe. W tym momencie już wiadomo orientacyjne czy tlenu jest dużo czy mało. Im osad bardziej brązowy tym tlenu jest więcej.
Zatykamy kolbkę korkiem nad zlewem bo trochę cieczy się wyleje i mieszamy intensywnie by cały tlen przereagował z osadem wodorotlenku manganu, po wytrząsaniu kolbkę odstawiamy na jeszcze kilka min. aż osad opadnie na dno.

Rys: Opadanie osadu na dno.
Teraz dodajemy 1 cm3 stężonego kwasu siarkowego. Osad zaczyna się rozpuszczać i z dodanego wcześniej jodku potasu wydziela się wolny jod w ilości proporcjonalnej do zawartego w wodzie tlenu.

Rys: Rozpuszczanie osadu w kawasie siarkowym.
Kolbkę zamykamy i intensywnie mieszamy aż cały osad się rozpuści. Następnie wstawiamy ją w ciemne miejsce by cały jod się wydzielił.

Rys: Osad w trakcie mieszania i rozpuszczania w kwasie.
Po rozpuszczeniu osadu roztwór powinien być klarowny i zabarwiony na żółto od wydzielonego wolnego jodu. Im badana próbka zawierała więcej tlenu tym intensywność barwy będzie większa.

Rys: Osad rozpuścił się i wydzielił się z roztworu wolny jod, który zabarwił go na żółto.
Miareczkowanie i opracowanie wyników.
Gdy mamy już próbkę z wolnym jodem trzeba sprawdzić ile go się tam wydzieliło by na tej podstawie określić ilość tlenu. W tym celu, za pomocą pipety jednomiarowej pobieramy 25 cm3 roztworu i przenosimy do kolby stożkowej o poj. ok. 250 cm3. Jeśli próbka jest bardzo ciemna możemy ją trochę rozcieńczyć wodą destylowaną. Dodajemy kilka kropli roztworu skrobi, co powoduje zabarwienie roztworu na niebiesko.
Teraz pora ustawić biuretę w statywie i napełnić ją wcześniej przygotowanym roztworem tiosiarczanu sodu o stężeniu 0,025 mol x dm-3. Jeśli jest mokra, należy ją tym roztworem przepłukać pamiętając, że roztwór po płukaniu rozcieńczył się pozostałościami wody w biurecie i już się nie nadaje do oznaczeń. Należy też pamiętać by pod zaworem nie pozostał pęcherzyk powietrza i by menisk cieczy w biurecie znajdował się na wysokości kreski zerowej.

Rys. Biureta umieszczona w statywie, oraz stożkowa kolba z roztworem, który będziemy miareczkować.
Teraz kropla po kropli wpuszczamy do kolby tiosiarczan z biurety aż do momentu gdy roztwór się odbarwi, co będzie świadczyć o całkowitym przereagowaniu wolnego jodu, a ilość zużytego do reakcji tiosiarczanu jest proporcjonalna do ilości jodu a tym samym do ilości tlenu, który był rozpuszczony.
Teraz wystarczy przeprowadzić odpowiednie obliczenia. Do obliczenia ilości rozpuszczonego w wodzie tlenu (X) w mg(O2) x dm-3 zastosujemy poniższy wzór matematyczny:
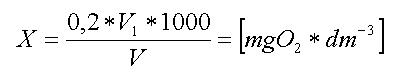
Gdzie:
V1 - objętość r-r mianowanego tiosiarczanu sodu o stężeniu równym 0,025 mol x dm-3 zużyta do zmiareczkowania wydzielonego jodu wyrażona w cm3
0,2 - ilość tlenu odpowiadąjaca 1 cm3 roztworu tiosiarczanu sodu o stężeniu dokładnie równym 0,025 mol x dm-3, wyrażona w mg
V - objętość próbki wody użytej do miareczkowania, w cm3
Do mojego miareczkowania wody pobranej ze stawu (temp. pobranej wody 19 oC) zużyłem 0,45 cm3 mianowanego r-r tiosiarczanu. Więc:
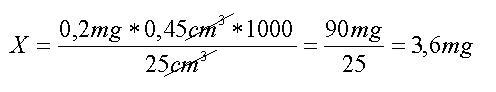
Z równania wynika, że woda w moim stawie zawiera 3,6 mg rozpuszczonego tlenu w 1 dm3


















